3D-Simulation eines PEM-Brennstoffzellen-Luft-Start-Szenarios einschließlich Degradation
Veröffentlicht: Dezember 17, 2025 · 10 Min. Lesezeit
Je nach Abschaltverfahren, Umgebungsdruckbedingungen und der Qualität der Dichtungen kann es mehrere Stunden bis Tage dauern, bis das Anodenkompartment vollständig mit Luft gefüllt ist. Dies stellt ein Problem beim anschließenden Startvorgang dar: Es wird eine Kohlenstoffkorrosion ausgelöst, die zu einer Verdünnung der Katalysatorschicht und Ablösung von Platinpartikeln führt – siehe Abbildung 1. Dadurch wird die Zellleistung und Lebensdauer reduziert. Details des zugrunde liegenden Prozesses während dieses Luft-(oder Luft/Luft)-Startvorgangs werden im nächsten Abschnitt beleuchtet.
![Carbon corrosion of the cathode catalyst layer (upper white stripe): begin of life (left); end of life (right) [1].](/sites/default/files/styles/original_small/public/2025-12/figure1_fuel-cell-startup.png.webp?itok=cvOwZy9B)
Wir gehen davon aus, dass das Anodenkompartment vollständig mit Luft gefüllt ist. Sobald die Brennstoffzelle erneut gestartet wird, beginnt Wasserstoff in die Anodenkanäle zu strömen. Aufgrund der vorhandenen Luft in den Anodenkanälen entwickelt sich eine Wasserstoff-/Luft-Front. Dies hat folgende Konsequenzen – siehe auch Abbildung 2: Nahe dem Anodeneinlass startet eine Wasserstoffoxidationsreaktion (HOR). Die dabei erzeugten Elektronen in der Nähe der H₂/O₂-Front fließen nicht wie üblich über einen äußeren Lastkreis, sondern lösen stattdessen eine Sauerstoffreduktionsreaktion (ORR) mit dem vorhandenen Sauerstoff aus, wo sie direkt verbraucht werden.
Da neben den Elektronen auch Wasserstoffprotonen in der ORR verbraucht werden, ändert sich die interne Zellstromrichtung: Protonen werden nun in „falscher“ Richtung transportiert, d.h. von der Kathode zur Anode. Dies führt dazu, dass das Kathodenpotenzial auf sehr hohe Werte (> 1,5 V) ansteigt, wodurch eine starke Kohlenstoffkorrosion (Carbon Oxidation Reaction, COR) der Kathodenkatalysatorschicht ausgelöst wird.
Bei so hohen Potenzialen kann es zudem zur Sauerstoffentwicklung (Oxygen Evolution Reaction, OER) kommen, wie sie normalerweise in Elektrolyseuren auftritt. Wie in Abbildung 2 zu sehen ist, ist die Zelle nun in einen aktiven Teil, der Strom erzeugt (links), und einen passiven Teil, der Strom verbraucht (rechts), unterteilt. Während des Startvorgangs wird der passive Teil nach und nach durch den aktiven Teil ersetzt.
![Figure 2: Mechanism of reverse-current decay during an air start-up [2].](/sites/default/files/styles/original_small/public/2025-12/figure2_fuel-cell-startup.png.webp?itok=odvZV6q6)
Neben den bereits erwähnten Reaktionen laufen gleichzeitig folgende Mechanismen ab:
- Platinoxidation: Bei den auftretenden Potenzialen spielt die Platinoxidation sowohl an der Kathode als auch an der Anode eine wichtige Rolle. Sie beeinflusst die lokalen Ströme und Spannungen erheblich, indem sie als pseudo-kapazitive Widerstandskomponente wirkt.
- Doppelschichtkapazität: Ein weiterer wichtiger kapazitiver Effekt entsteht durch das Auf- und Entladen der elektrochemischen Doppelschicht, das ebenfalls sowohl an der Kathode als auch an der Anode stattfindet.
Ein ähnliches Szenario kann auch beim Abschalten einer PEM-Brennstoffzelle auftreten.
Alle im vorherigen Abschnitt erwähnten Reaktionen finden innerhalb der Anoden- oder Kathodenkatalysatorschicht statt. Daher ist es wichtig, die Katalysatorschichten lokal aufzulösen, wie es üblicherweise in AVL FIRE™ M erfolgt. Abbildung 3 zeigt eine typische Diskretisierung der Katalysatorschichten und der Membran, also einen Teil des Rechennetzes, zusammen mit den gelösten Reaktionsgleichungen und dem Transport durch die Membran.
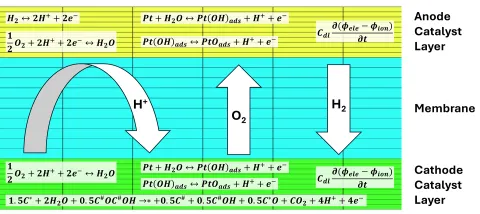
Die Reaktionen erzeugen lokale Massen-, Wärme- und Stromquellen, wodurch lokal die Gaskomponentenanteile, Temperatur und Potenzial verändert werden. In der Membran wird der protonische Strom durch die Stromquellen in den Katalysatorschichten bestimmt, was zu einer 3D-Ionenpotenzialverteilung führt. Gaskomponenten werden ebenfalls durch die Membran transportiert, z. B. wird die Wasserstoffkonzentration an der Anode zusätzlich durch den Wasserstoff-Crossover von der Anode zur Kathode beeinflusst.
Der Transport der Gaskomponenten von den Kanälen über die Gasdiffusionsschichten zu den Katalysatorschichten erfolgt wie gewohnt. Ein wichtiger Unterschied zu einer „standardmäßigen“ Brennstoffzellensimulation ist der hochdynamische Prozess, im Gegensatz zu der üblicherweise betrachteten stationären Bedingung. In diesem Zusammenhang ist es entscheidend, dass jeder Zeitschritt mit ausreichender Genauigkeit konvergiert und dass die verwendete Zeitschrittgröße zum Problem passt. Letzteres kann durch die Anwendung einer adaptiven Zeitschrittgröße erreicht werden.
Ein Vergleich mit realen Daten ist unerlässlich, um die Genauigkeit mathematischer Modelle zu bewerten. Ein häufiges Problem bei der Validierung elektrochemischer Modelle für Brennstoffzellen und Elektrolyseure ist die geringe Verfügbarkeit von Messdaten. Die meisten berechneten Ergebnisgrößen können schlichtweg nicht gemessen werden. Daher ist es oft notwendig, sich auf globale Größen wie Strom, Spannung oder Temperatur zu stützen.
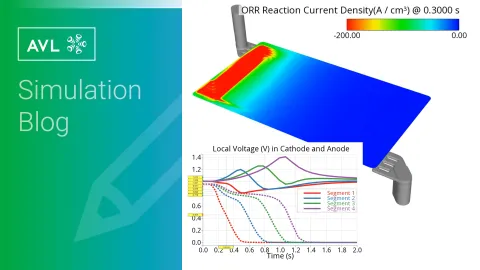
Jede Reaktion, die während des Luft-Startvorgangs abläuft, erzeugt einen elektrischen Strom, der die lokale Spannung beeinflusst. Abbildung 4 zeigt die unterschiedlichen Strombeiträge auf der Kathoden- und Anodenseite in den Segmenten einer Zelle mit geraden Kanälen.
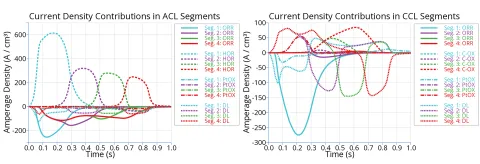
Die Summe dieser Ströme und die resultierende lokale Spannung können mit Messdaten verglichen werden. Abbildung 5 zeigt die lokale Spannung an Kathode und Anode sowie die Stromdichte in Simulation und Messung [3] in vier Segmenten, wobei Segment 1 und 4 am Anodeneinlass bzw. -auslass liegen.
Obwohl die Übereinstimmung nicht perfekt ist, können die wichtigsten Trends durch die Simulation vorhergesagt werden:
- Die maximale lokale Spannung tritt an der Kathode mit einem Wert von ca. 1,6 V auf.
- Die gesamte Start-up-Zeit beträgt etwa 1 s.
- Das höchste Kathodenpotenzial tritt in Segment 4 auf, also nahe dem Anodenauslass.
Segment 1 zeigt die höchste negative Stromdichte (Arbeitsrichtung: Protonen von Anode zu Kathode) und Segment 4 die höchste positive Stromdichte (Richtung umgekehrt: Protonen von Kathode zu Anode).
Das hohe Kathodenpotenzial am Anodenauslass verstärkt die lokale Kohlenstoffkorrosionsrate, wie im nächsten Abschnitt gezeigt wird.
![Figure 5: Local voltage in cathode and anode (top) and current density (bottom) in simulation (left) and experiment [3] (right); the results are shown in four segments along the anode channel.](/sites/default/files/styles/original_small/public/2025-12/figure5_fuel-cell-startup.png.webp?itok=UzGhMnYY)
Die Anwendung des Modells auf eine industrielle PEM-Brennstoffzelle liefert interessante Einblicke in das lokale Verhalten während der Start-up-Phase. Abbildung 6 zeigt den Transport von Wasserstoff und Sauerstoff durch die Anodenkanäle und die Anodenkatalysatorschicht. Der Austausch von Sauerstoff durch Wasserstoff ist nach ca. 3 Sekunden abgeschlossen.

Abbildung 7 zeigt die HOR- und ORR-Stromdichten in der Anodenkatalysatorschicht während der ersten 2 Sekunden nach Beginn der Wasserstoffinjektion. Die Reaktionsraten erreichen ihren Höhepunkt an der H₂/O₂-Front. Die Front liegt unter den äußersten Kanälen aufgrund des verbesserten H₂- und O₂-Transports in der Gasdiffusionsschicht (GDL), der durch den großen Druckgradienten zwischen benachbarten Kanälen entsteht.

Abschließend werden in Abbildung 8 die lokale Spannung und die Kohlenstoffkorrosionsrate in der Kathodenkatalysatorschicht während der ersten 3 Sekunden gezeigt. Während die H₂/O₂-Front durch die Zelle wandert, steigt die lokale Kathodenspannung. Der Bereich in der Nähe des Anodenauslasses ist über einen längeren Zeitraum O₂ ausgesetzt. Daher steigt dort die lokale Spannung auf hohe Werte, was zu einer hohen lokalen Kohlenstoffkorrosionsrate führt.

Mit der Version 2025 R2 von FIRE M kann ein realistisches Luft-Start-Szenario einer PEM-Brennstoffzelle simuliert werden. Während des Startvorgangs spielen parasitische Redoxreaktionen, Platinoxidation, Kohlenstoffkorrosion und die Doppelschichtkapazität eine zentrale Rolle. Die resultierenden lokalen Ströme und Spannungen sind mit Messdaten vergleichbar.
Der kritischste Bereich ist der Anodenauslass, wo das lokale Kathodenpotenzial sehr hohe Werte erreicht, was zu starker Kohlenstoffkorrosion führt. 3D-Ergebnisse können genutzt werden, um das lokale Verhalten während des transienten Prozesses zu analysieren. Die transiente 3D-Simulation ermöglicht unter anderem die Analyse des Fortschreitens der Wasserstoff-/Sauerstoff-Front sowie der Lage und des Beginns der resultierenden Kohlenstoffkorrosionsrate.
Mit Hilfe solcher Ergebnisse können Geometrie und Betriebsbedingungen optimiert werden, um die Degradation während der Start-up-Phase zu minimieren.
[1] G. M. Carrabba et al., Int. J. Hydrogen Energy 133, 546, 2025.
[2] R. B. Kaspar et al., J. Electrochem. Soc. 163, F377, 2016.
[3] E. Colombo et al., J. Electrochem. Soc. 168, 054508, 2021.
Bleiben Sie auf dem Laufenden
Verpassen Sie keinen Teil unserer Simulation-Blogreihe – jetzt anmelden!
Folgen Sie unserem Simulation-Blog
Bleiben Sie auf dem Laufenden mit unserer Simulation-Blogreihe – jetzt anmelden!