3D-Modellierung der Co-Elektrolyse in Festoxid-Elektrolyseuren: Ein Weg zu klimaneutralen Kraftstoffen
Veröffentlicht: November 03, 2025 · 2 Min. Lesezeit
Eine Festoxid-Elektrolysezelle arbeitet typischerweise bei Temperaturen zwischen 700 und 900 °C, bei denen die Ionenleitfähigkeit im Festoxid-Elektrolyten außerordentlich hoch ist und damit die thermodynamische Effizienz maximal ist. Die Zelle besteht aus drei Funktionsschichten: der Kathode, dem Elektrolyten und der Anode.
Die Kathode, auch als Brennstoffelektrode bezeichnet, besteht in der Regel aus einem Nickel-Yttrium-stabilisierten Zirkonoxid (Ni-YSZ)-Cermet, das sowohl elektronische Leitfähigkeit als auch katalytische Aktivität bietet. An dieser Elektrode finden die wichtigsten Reduktionsreaktionen statt. Wenn ein Gemisch aus Kohlendioxid, Wasserdampf und Wasserstoff in den Kathodenkanal eingespeist wird, treibt die zugeführte elektrische Energie die elektrochemische Reduktion von CO₂ und H₂O an. Die beiden wichtigsten elektrochemischen Reaktionen, die an der Kathode ablaufen, sind die Reduktion von Wasserdampf zu Wasserstoff
und die Reduktion von Kohlendioxid zu Kohlenmonoxid.
Die bei diesen Reaktionen entstehenden Oxidionen (O²⁻) werden durch die dichte Elektrolytschicht geleitet, die typischerweise aus einer dünnen Schicht aus gadoliniumdotiertem Ceroxid (GDC) und yttriumstabilisiertem Zirkonoxid (YSZ) besteht. Der Elektrolyt ist für Gase undurchlässig, ermöglicht jedoch den selektiven Transport von Oxidionen von der Kathode zur Anode.
An der Anode, die häufig aus Lanthan-Strontium-Manganat (LSM) oder Lanthan-Strontium-Kobaltferrit (LSCF) besteht, werden diese Oxidionen gemäß
zu molekularem Sauerstoff oxidiert. Die dabei freigesetzten Elektronen werden über den externen Stromkreis zur Kathode zurückgeführt, wodurch der elektrochemische Kreislauf geschlossen wird. Als Spülgas auf der Anodenseite wird in der Regel Luft verwendet, wodurch ein mit Sauerstoff angereicherter Abgasstrom entsteht.
Parallel zu den elektrochemischen Reaktionen findet innerhalb der porösen Nickel-Katalysatorschicht der Kathode eine thermochemische Gleichgewichtsreaktion statt, die als Wasser-Gas-Shift-Reaktion (WGSR) bekannt ist. Diese Reaktion
wandelt Wasserstoff und Kohlenmonoxid um und stellt ein Gleichgewicht her, das zur Anpassung der Synthesegaszusammensetzung beiträgt. Bei den für den SOEC-Betrieb typischen erhöhten Temperaturen verschiebt sich das Gleichgewicht in Richtung der CO-Produktion und ergänzt so die elektrochemische Reduktion von CO₂.
Das in die Kathode eintretende Gasgemisch enthält typischerweise CO₂, H₂O und eine geringe Menge H₂. Der Wasserstoff dient dazu, eine reduzierende Umgebung aufrechtzuerhalten, welche die Oxidation des Nickel-Katalysators verhindert. Während die Gase durch die poröse Kathode strömen, werden CO₂ und H₂O elektrochemisch reduziert, und zusammen mit der Gleichgewichtsverschiebung aus der WGSR wird der austretende Gasstrom mit H₂ und CO angereichert. Folglich besteht der Kathodenausfluss hauptsächlich aus Synthesegas (H₂ + CO) zusammen mit Restmengen an H₂O und CO₂, während auf der Anodenseite Sauerstoff entsteht.
Dieser Prozess kombiniert elektrochemische und thermochemische Prozesse und ermöglicht so eine effiziente Umwandlung von elektrischer und thermischer Energie in chemische Brennstoffe. Durch Anpassung der Einlassgasverhältnisse, der Betriebstemperatur und der Stromdichte kann das H₂/CO-Verhältnis des erzeugten Synthesegases präzise auf die Anforderungen der nachgeschalteten Synthese abgestimmt werden.
Wasser-Gas-Shift-Reaktion
Innerhalb von FIRE M wird die Wasser-Gas-Shift-Reaktion (WGSR) direkt in der Kathodenelektrode implementiert, siehe Abbildung 1. Diese Reaktion spielt eine entscheidende Rolle bei der Bestimmung der lokalen Synthesegaszusammensetzung und bei der Kopplung der chemischen und elektrochemischen Teilsysteme. Um die Versuchsbedingungen genau widerzuspiegeln, können die WGSR-Parameter automatisch an die Versuchsmessungen angepasst werden, wodurch eine realistische Darstellung der Gleichgewichts- und Kinetikeffekte innerhalb der porösen Ni-basierten Kathode gewährleistet wird. Auf diese Weise können Anwender das Modell auf bestimmte Zellmaterialien, Temperaturen und Gaszusammensetzungen kalibrieren und so die Vorhersagegenauigkeit von Co-Elektrolyse-Simulationen verbessern.

Elektrochemische Reaktionen
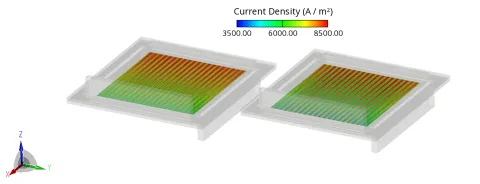
Alle elektrochemischen Modelle in FIRE M sind als Grenzflächenreaktionen zwischen den Elektroden und dem Elektrolyten sowie als volumetrische (3D) Reaktionen formuliert, die innerhalb der porösen Elektroden verteilt sind. Dieser duale Ansatz bietet Flexibilität bei der Darstellung verschiedener physikalischer Zustände. Für Systeme, bei denen die Ionenleitfähigkeit innerhalb der Elektroden sehr gering ist, ist das Grenzflächenmodell in der Regel besser geeignet, da die elektrochemische Aktivität auf die Grenze zwischen Elektrode und Elektrolyt beschränkt ist. Umgekehrt erfasst das 3D-Volumenmodell bei Elektroden mit ausreichender Ionen- und Elektronenleitfähigkeit die räumliche Verteilung der elektrochemischen Aktivität in der gesamten porösen Struktur und liefert eine realistischere Beschreibung der Stromdichte und der Potentialfelder (siehe Abbildung 2).

3D-Reaktionszone
Basierend auf Erkenntnissen aus Mikrosimulationsstudien, die zeigten, dass ein volumetrischer Ansatz neben dem Grenzflächenansatz unerlässlich ist, um das Verhalten elektrochemischer Reaktionen in porösen Elektroden realistisch zu erfassen, wurde eine volumetrische Reaktionszone eingeführt.
Die Entscheidung, die Reaktionszone von 2D auf 3D zu erweitern, basierte auf mikrostrukturellen Simulationsarbeiten, die im Rahmen des FFG-Projekts „Design-SOEC“ gemeinsam mit der Montanuniversität Leoben und dem Material Center Leoben durchgeführt wurden. In diesem Projekt wurden 3D-Mikrostrukturdaten der Luftelektrode vom Material Center Leoben bereitgestellt. Die 3D-Morphologie wurde aus FESEM-Bildern (Feldemissions-Rasterelektronenmikroskopie) mithilfe einer KI-basierten Bildverarbeitung rekonstruiert. Aus dieser rekonstruierten Mikrostruktur wurde ein repräsentativer 3D-Schnitt einer Knopfzelle erstellt, wobei die Luftelektrode vollständig dreidimensional aufgelöst wurde (siehe Abbildung 3).
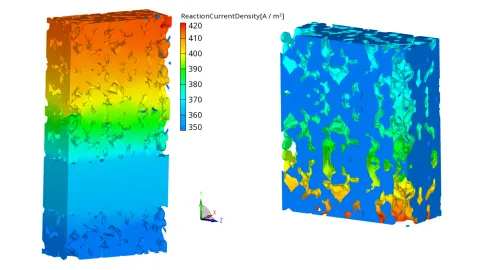
Die FIRE M Simulationsplattform wurde entsprechend angepasst und erweitert, um diesen mikrostrukturellen Ausschnitt zu simulieren. Diese Bemühungen bestätigten, dass lokale Reaktionsgeschwindigkeiten und Stromverteilungen durch rein zweidimensionale Modelle nicht genau genug dargestellt werden können – insbesondere bei heterogenen Elektroden mit unterschiedlicher Porosität und Tortuosität. Folglich umfasst die neue 3D-Reaktionszonenimplementierung die Ionenleitfähigkeit in porösen Feststoffen und eine volumetrische Austauschstromdichte, wodurch FIRE M den 3D-Ionentransport simulieren und die räumliche Verteilung der Reaktionsstellen in der gesamten elektrochemisch aktiven Schicht erfassen kann. Mit dieser Erweiterung konnte eine bessere Annäherung an die gemessene VI-Kurve für eine Knopfzelle erzielt werden, siehe Abbildung 4.

Gekoppelte Maxwell-Stefan- und Knudsen-Diffusion
Die genaue Vorhersage des Gastransports in porösen Elektroden ist für die SOEC-Modellierung von entscheidender Bedeutung. FIRE M enthält eine detaillierte Mehrkomponenten-Diffusionsformulierung, welche die Maxwell-Stefan-Diffusion mit Knudsen-Diffusionseffekten konsistent kombiniert. Diese Entwicklung war besonders anspruchsvoll, da sie die Ableitung eines konsistenten mathematischen Rahmens erforderte, der gleichzeitig die molekulare Diffusion, die Wechselwirkung zwischen Spezies und die Einschränkungseffekte auf Porenebene berücksichtigt. Die daraus resultierende Implementierung ermöglicht es FIRE M, den Gastransport auch in Elektroden mit sehr feinen Poren genau darzustellen, wo Knudsen-Effekte signifikant werden und lokale Reaktionsgeschwindigkeiten und Speziesgradienten stark beeinflussen können (siehe Abbildung 5).
FIRE M vereint die CO₂ + H₂O Co-Elektrolyse und kombiniert die elektrochemische Reduktion von Wasserdampf und Kohlendioxid mit der Wassergas-Shift-Reaktion innerhalb der porösen Nickel-basierten Elektrode. Mit fortschrittlicher 3D-Reaktionszonenmodellierung, volumetrischer elektrochemischer Kinetik, Mehrkomponenten- und Knudsen-Diffusion liefert die aktuelle Version von FIRE M eine noch höhere Genauigkeit für die Synthesegaszusammensetzung und Prozesssimulation.
Bleiben Sie auf dem Laufenden
Verpassen Sie keinen Teil unserer Simulation-Blogreihe – jetzt anmelden!
Folgen Sie unserem Simulation-Blog
Bleiben Sie auf dem Laufenden mit unserer Simulation-Blogreihe – jetzt anmelden!